Podsumowanie wiadomości z fizyki jądrowej
W tym dziale przedstawiliśmy zbiór elementarnych wiadomości dotyczących budowy i właściwości jądra atomowego. Opisaliśmy procesy zwane przemianami promieniotwórczymi – rozpady jądrowe, reakcje jądrowe, rozszczepienia jądra. Przeanalizowaliśmy sposoby wyzwalania energii jądrowej i wyjaśniliśmy pojęcia deficytu masy i energii wiązania. Zdefiniowaliśmy okres połowicznego zaniku i sformułowaliśmy prawo rozpadu promieniotwórczego. Scharakteryzowaliśmy promieniowanie jądrowe i jonizujące. Opisaliśmy również sposoby ich wykrywania oraz to, jak można się przed nimi chronić.

1. Jądro atomu

Jądrem atomowym nazywamy element znajdujący się w centralnej części atomu.
Jądro atomowe jest bardzo małe (kilkadziesiąt tysięcy razy mniejszy od atomu).
Jądro atomowe skupia praktycznie całą masę atomu.
Jądro atomowe obdarzone jest ładunkiem dodatnim.
Jądro atomowe składa się z protonów i neutronów, czyli nukleonów. Protony obdarzone są ładunkiem dodatnim, a neutrony są elektrycznie obojętne. Masy tych cząstek mają zbliżoną wartość.
Skład jądra atomowego zapisujemy jako:
gdzie:
– symbol chemiczny pierwiastka;
– liczba porządkowa zawierająca informację, o liczbie protonów w jądrze;
– liczba masowa równa liczbie nukleonów w jądrze;
– liczba neutronów w jądrze.
– jądro izotopu potasu zawiera 19 protonów i 21 neutronów, czyli razem 40 nukleonów.
2. Izotopy

Izotopami nazywamy odmiany atomów tego samego pierwiastka różniące się masą.
Jądra izotopów mają taką samą liczbę protonów (liczba ), różną liczbę neutronów, a tym samym różną liczbę masową ().
Izotopy danego pierwiastka mają takie same właściwości chemiczne, ale różne właściwości fizyczne.
Pierwiastki naturalnie występujące w przyrodzie są mieszaniną wielu izotopów, choć poszczególne izotopy mogą mieć różny udział w tej mieszaninie. Przykładowo: w naturalnie występującym wodorze, będącym mieszaniną trzech izotopów: , , , pierwszy z nich stanowi składu tego pierwiastka.
3. Defekt masy

Defektem (deficytem) masy nazywamy różnicę między sumą mas nukleonów (gdy są one poza jądrem) tworzących jądro a masą tego jądra.
oznacza masę jądra o liczbie masowej i liczbie porządkowej .
Suma mas jego składników to:
Defekt masy to:
4. Energia wiązania

Między nukleonami działają siły jądrowe. Siły te:
nie zależą od ładunku elektrycznego;
mają dużą wartość (znacznie większą od sił grawitacyjnych i elektrostatycznych);
mają krótki zasięg (działają na małych odległościach).
W wyniku działania sił jądrowych nukleony są ze sobą związane. O tym, jak silne jest to wiązanie, mówi nam energia wiązania – jest ona równa pracy, jaką należy wykonać, aby rozłożyć jądro na pojedyncze nukleony.
Obliczenie energii wiązania umożliwia zasada równoważności masy i energii:
,
gdzie:
– masa;
– prędkość światła w próżni;
– energia, jaką można uzyskać z masy .Energia wiązania jest równa energii równoważnej deficytowi masy:
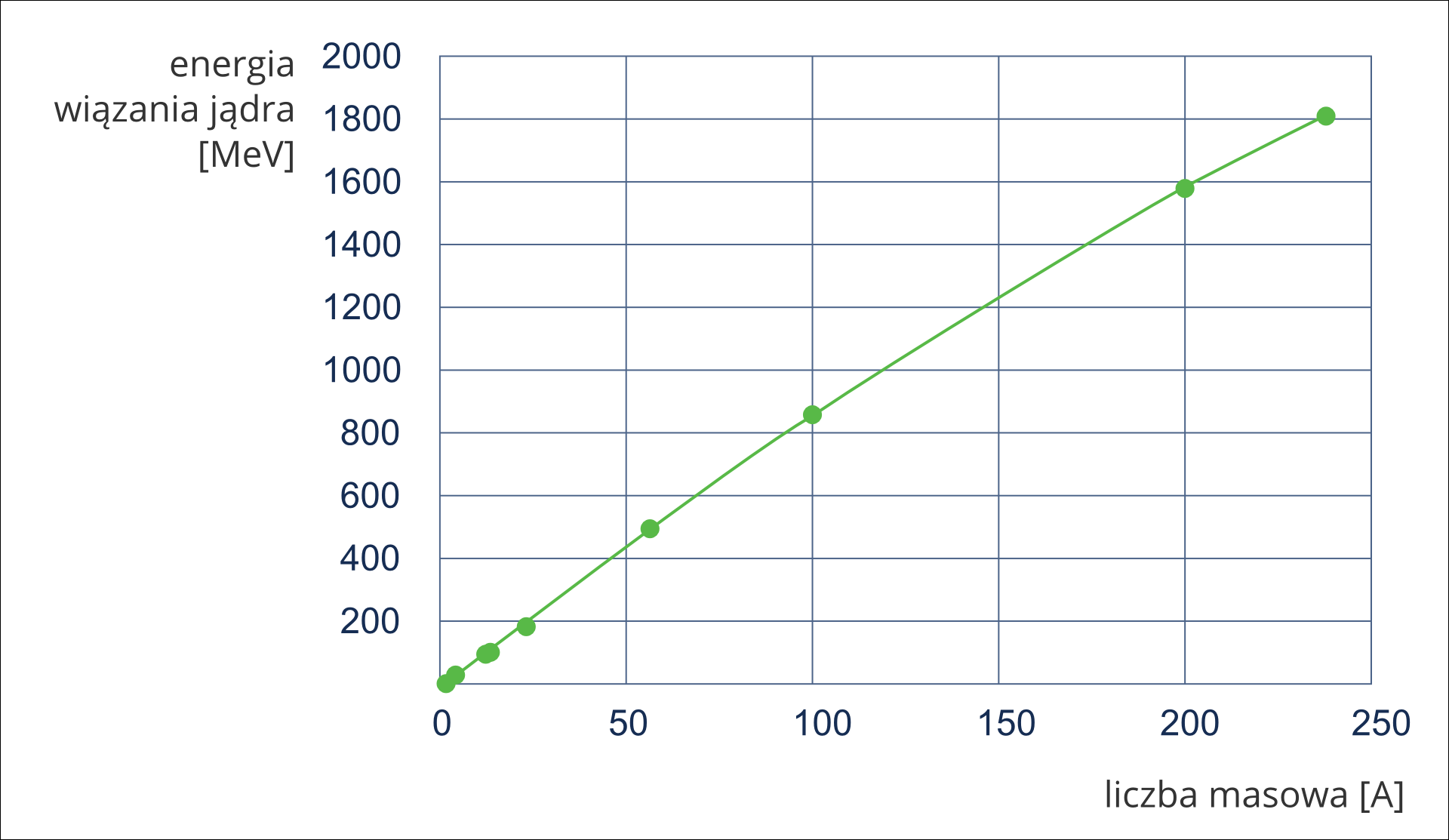
Energia wiązania jądra rośnie wraz z liczbą masową atomuEnergia wiązania jądra rośnie wraz z liczbą masową atomu.
Ważną charakterystyką jądra każdego izotopu dowolnego pierwiastka jest energia wiązania przypadająca na jeden nukleonWażną charakterystyką jądra każdego izotopu dowolnego pierwiastka jest energia wiązania przypadająca na jeden nukleon.
5. Promieniowanie jądrowe
Promieniowanie emitowane przez substancje zawierające niestabilne jądra izotopów naturalnych podzielono na trzy kategorie: , i .
Promieniowanie to strumień cząstek, składających się z dwóch protonów i dwóch neutronów (a więc tak samo jak jądra helu). Ładunek cząstki wynosi +2 e (e – ładunek elementarny). Charakteryzuje się niską przenikliwością – jego zasięg w powietrzu nie przekracza 10 cm. Promieniowane ma właściwości jonizujące i jego kontakt z żywą tkanką prowadzi do jej uszkodzeń.
Promieniowanie to strumień elektronów, którego przenikliwość jest większa niż cząstek alfa – rozchodzi się na odległość nawet do kilku metrów. Ma własności jonizujące, podobnie jak promienie .
Promieniowanie jest falą elektromagnetyczną o długości mniejszej lub równej długości fal promieniowania rentgenowskiego. Jest to promieniowanie najbardziej przenikliwe; w powietrzu rozchodzi się na odległość od kilku do kilkunastu metrów, a w wodzie – na ponad 1 metr. Jest promieniowaniem jonizującym.

Ponadto jądra sztucznie wytworzonych izotopów mogą emitować:
Cząstki – pozytony, czyli dodatnie elektrony. Zasięg ich nie jest duży, ale pozytony w wyniku zderzania się z elektronami ulegają anihilacji i powstaje wtedy promieniowanie gamma.
Neutrony – przenikliwe, obojętne elektrycznie cząstki. Neutrony łączą się z jądrami atomów i przekształcają je w niestabilne jądra promieniotwórcze.
Protony (p) – dodatnio naładowane cząstki o właściwościach zbliżonych do promieniowania , jednak znacznie bardziej od nich przenikliwe.
6. Dawka promieniowania
Aby określić parametry promieniowania i skalę efektów wywołanych przez promieniowanie w ośrodku materialnym, wprowadzono następujące definicje:
Aktywność preparatu promieniotwórczego () – liczba jąder promieniotwórczych ulegających przemianom jądrowym w ciągu sekundy. Jednostką aktywności preparatu promieniotwórczego jest bekerel (). oznacza jeden rozpad jądra w ciągu sekundy.
Dawka pochłonięta () – energia promieniowania pochłonięta przez jednostkę masy substancji. Jednostką dawki pochłoniętej jest grej (Gy); .
Równoważnik dawki () – iloczyn dawki pochłoniętej () i współczynnika jakości promieniowania (). Służy do oceny wpływu promieniowania na układy biologiczne. Jednostką równoważnika dawki jest siwert (; .
Współczynnik jakości () jest definiowany przez porównanie skutków danego rodzaju promieniowania ze skutkami promieniowania wzorcowego o tej samej dawce pochłoniętej. Wartość współczynnika jakości mieści się w zakresie od 1 do 25.
7. Okres połowicznego rozpadu

Okres (czas) połowicznego rozpadu (zaniku) – czas, po którym z początkowej liczby jąder promieniotwórczych pozostanie połowa z nich.
Okres połowicznego rozpadu oznaczany jest symbolem lub . Jest wielkością charakterystyczną dla konkretnego izotopu pierwiastka.
Okres połowicznego rozpadu może przyjmować wartości od ułamków mikrosekundy do miliardów lat.
Przykładowo: okres połowicznego rozpadu radonu wynosi 4 dni. Oznacza to, że po upływie 4 dni zostanie tylko połowa początkowej liczby jąder tego gazu, po upływie kolejnych 4 dni – połowa z połowy, czyli jedna czwarta, a po następnych 4 dniach – połowa z jednej czwartej itd.
8. Prawo rozpadu promieniotwórczego

Rozpad jąder promieniotwórczych ma charakter przypadkowy i podlega prawom statystyki. Oznacza to, że jeśli znamy okres połowicznego zaniku, możemy oszacować, jaka liczba jąder rozpadnie się w pewnym przedziale czasu. Nie możemy jednak przewidzieć, które z tych jader się rozpadną i kiedy rozpadnie się jedno konkretne jądro. Poniższe równanie, zwane prawem rozpadu promieniotwórczego, pozwala obliczyć liczbę jąder promieniotwórczych, które pozostały po upływie czasu ():
gdzie:
– początkowa liczba jąder;
– okres połowicznego zaniku.
9. Przemiany jądrowe

Emisja promieniowania jądrowego jest następstwem przemian zachodzących w jądrach atomów. Przemiany te opisuje się za pomocą równań podobnych do równań reakcji chemicznych, choć rozpady promieniotwórcze nie są reakcjami chemicznymi, lecz procesami fizycznymi.
Wszystkie przemiany jądrowe odbywają się z zachowaniem następujących zasad:
Zasada zachowania liczby nukleonów – suma liczby nukleonów we wszystkich produktach rozpadu jest równa liczbie nukleonów przed rozpadem.
Zasada zachowania ładunku – suma ładunków w produktach rozpadu jest po rozpadzie taka sama jak przed rozpadem.
Zasada masy i energii – suma mas i energii po rozpadzie jest taka sama jak przed rozpadem.
Rozpad polega na wyrzuceniu z wnętrza jądra cząstki złożonej z dwóch protonów i dwóch neutronów. Tę cząstkę nazywamy cząstką . W efekcie powstaje jądro innego pierwiastka, którego liczba masowa jest mniejsza o 4, a liczba porządkowa – o 2.
Rozpad polega na emisji elektronu z wnętrza jądra. Związane jest to z przekształceniem się jednego z neutronów w proton. W rezultacie proton pozostaje w jądrze, którego liczba porządkowa wzrasta o 1, a jądro jednocześnie zachowuje poprzednią wartość liczby masowej. Jądro ulega przemianie w nowe jądro.
Rozpad polega na emisji pozytonu (antyelektronu) z wnętrza jądra. Związane to jest z przekształceniem się jednego protonu w neutron, który pozostaje w jądrze.
Rozpad przemiana, której podlega jądro znajdujące się w stanie wzbudzonym. W takim jądrze znajduje się nadmiar energii; aby się go pozbyć, jądro wysyła foton promieniowania . W wyniku tej przemiany skład jądra się nie zmienia. Przemiana ta często następuje po wcześniejszej przemianie .
10. Reakcje jądrowe
Bombardowanie jąder atomów strumieniem cząstek alfa, protonów lub neutronów (a obecnie często jądrami innych atomów) oraz promieniowaniem gamma prowadzi do przekształcenia tych cząstek w jądra innych pierwiastków. Temu procesowi towarzyszy emisja promieniowania. Takie sprowokowane przemiany jądrowe nazywamy reakcjami jądrowymi. Można je zapisać za pomocą wzoru:
gdzie:
– cząstka (pocisk) padającego promieniowania;
– atom bombardowany (tarcza);
– powstałe jadro;
– promieniowanie emitowane.
Przykłady:
lub
Takie reakcje wykorzystywane są do produkcji syntetycznych nuklidów promieniotwórczych wykorzystywanych w przemyśle, medycynie i technice. Dzięki drugiej z pokazanych reakcji wytworzono nowy pierwiastek – kopernik (Cn).
11. Rozszczepienie jądra atomowego
Rozszczepienie jąder ciężkich (w praktyce są to jądra uranu lub plutonu) na dwa lżejsze jądra to jeden ze sposobów wyzwalania energii jądrowej. Proces ten inicjowany jest bombardowaniem jąder ciężkich neutronami termicznymi. Neutron dołączony do jądra sprawia, że staje się ono niestabilne i w efekcie prowadzi do rozerwania jądra na dwa mniejsze. Podczas takiego procesu uwalniana jest energia oraz 2 lub 3 neutrony, które mogą inicjować rozszczepienie kolejnych jąder.
Przykładowy proces rozszczepienia jądra plutonu wygląda następująco:

12. Reakcja łańcuchowa
Reakcja łańcuchowa zachodzi samorzutnie; składają się na nią zachodzące kolejno reakcje rozszczepienia. Każda reakcja rozszczepienia wytwarza co najmniej dwa neutrony; cząstki te bombardują sąsiednie jądra. Neutrony zostają pochłonięte przez jądra, które się rozpadają i wytwarzają następne neutrony. Proces zachodzi lawinowo w całej objętości substancji.
Reakcji łańcuchowej towarzyszy wydzielanie olbrzymich ilości energii będącej skutkiem deficytu masy. W wyniku reakcji rozszczepienia jednego jądra uranu wydziela się energia wynosząca około 200 MeV.
Reakcja łańcuchowa nie zachodzi w każdych warunkach. Materiał rozszczepialny musi przekroczyć masę krytyczną. Jej istnienie jest spowodowane ucieczką neutronów poza objętość substancji; masa krytyczna zależy więc od rozmiarów i kształtu substancji.
13. Elektrownia jądrowa

Elektrownie jądrowe działają podobnie jak konwencjonalne elektrownie cieplne; różnica polega na sposobie uzyskiwania energii.
Energię cieplną wytwarzaną przez reaktor elektrownie jądrowe wykorzystują do zamiany wody w parę wodną. Ta napędza wirniki turbin i tak powstaje prąd elektryczny.
Reaktor jądrowy (zwany też dawniej stosem atomowym) jest urządzeniem przeznaczonym do sterowania przebiegiem reakcji jądrowych.
Nazwa | Funkcja | Najczęściej stosowane materiały |
paliwo | materiał rozszczepialny | wzbogacony uran, pluton |
moderator | spowalnia neutrony bez ich pochłaniania | woda, ciężka woda, grafit, beryl |
reflektor | kieruje neutrony ponownie do rdzenia | grafit |
chłodziwo | odprowadza ciepło z rdzenia reaktora | woda, powietrze, ciekły sód |
pręty kontrolne i pręty bezpieczeństwa | silnie pochłaniają neutrony | kadm, bor |
osłona biologiczna | chroni otoczenie przed promieniowaniem | beton zawierający dużo boru |
14. Synteza termojądrowa
Synteza termojądrowa to jeden ze sposobów wyzwalania energii jądrowej. Polega na łączeniu się lekkich jąder atomów w jądra cięższe. Aby zapoczątkować taki proces, należy jądra lekkie zbliżyć do siebie na tak małą odległość, aby zaczęły działać siły jądrowe. Aby pokonać siły elektrostatycznego odpychania, które się wytworzyły w wyniku zbliżania jąder, trzeba rozpędzić lekkie jądra i zderzyć je ze sobą. Taki proces zachodzi wyłącznie w bardzo wysokiej temperaturze (ponad milion kelwinów) – dlatego w nazwie reakcji znajduje się przedrostek „termo”.
Procesy syntezy termojądrowej zachodzą:
– we wnętrzach gwiazd, również w naszym Słońcu;
– w bombach wodorowych;
– w reaktorach termojądrowych (jak dotąd tylko eksperymentalnych, niemających zastosowań przemysłowych).

15. Detekcja promieniowania

Urządzenia służące do wykrywania i rejestrowania promieniowania jądrowego (jonizującego) nazywamy detektorami cząstek. Najczęściej są to urządzenia wykorzystujące:
– jonizację gazu (komora jonizacyjna, komora Wilsona, komora pęcherzykowa, licznik Geigera‑Müllera);
– pobudzanie pewnych substancji do świecenia (licznik scyntylacyjny);
– reakcje chemiczne (emulsja fotograficzna).
16. Promieniotwórczość w technice i medycynie

Sztuczna promieniotwórczość znalazła zastosowanie w wielu dziedzinach:
Energetyka – elektrownie, baterie jądrowe (używane np. do rozruszników serca).
Medycyna – radioizotopy, znaczniki do badań diagnostycznych, leczenie chorób nowotworowych (bomba kobaltowa), akceleratory.
Nauka – określanie wieku znalezisk archeologicznych metodą datowania radiowęglowego (datowanie izotopem Indeks górny 1414C), analiza aktywacyjna (bardzo czuła metoda badania składu pierwiastkowego próbki).
Technika – silniki atomowe okrętów i statków kosmicznych, precyzyjne grubościomierze, świecące farby, czujniki dymu.
Przemysł – wykrywanie defektów w elementach silników samolotowych, sterylizacja żywności i sprzętu medycznego, kontrola terminu ważności produktów.
Test
Przed rozpoczęciem rozwiązywania testu przygotuj kartkę i przybory do pisania.
Oceń prawdziwość poniższych zdań.
| Prawda | Fałsz | |
| Jeśli do jądra atomu pewnego pierwiastka dołączymy proton, to powstanie izotop tego pierwiastka. | □ | □ |
| Jeśli do jądra atomu pewnego pierwiastka dołączymy neutron, to powstanie izotop tego pierwiastka. | □ | □ |
| Tryt jest izotopem wodoru, a jego jądro zawiera 1 proton i dwa neutrony. | □ | □ |
| Jeśli w ciągu 3 godzin rozpada się połowa jąder izotopu promieniotwórczego, to po upływie 6 godzin rozpadną się wszystkie jądra tego izotopu. | □ | □ |
| Reakcje jądrowe są reakcjami chemicznymi. | □ | □ |
| Promieniowanie jonizujące jest szkodliwe i nie ma żadnych pożytecznych zastosowań. | □ | □ |
Z ilu protonów i neutronów składa się jądro ołowiu ?
- Z 82 protonów i 126 neutronów.
- Z 82 protonów i 208 neutronów.
- Z 126 protonów i 82 neutronów.
- Z 208 protonów i 82 neutronów.
- Z 82 protonów i 290 neutronów.
Które z równań poprawnie opisuje rozpad dla izotopu neodymu?
Które z równań poprawnie opisuje rozpad dla izotopu fosforu ?
Poniższe równanie opisuje jedną z możliwych reakcji rozszczepienia jądra uranu:
.
Jakie wartości mają: liczba masowa A i liczba porządkowa Z, powstałego tu izotopu baru ?
-
Z = 56
A = 139 -
Z = 8
A = 139 -
Z = 139
A = 58 -
Z = 56
A = 85 -
Z = 85
A = 56 -
Z = 58
A = 83
Podziel źródła promieniowania jonizującego na naturalne i sztuczne.
radio, broń jądrowa, cyklotron, farby świecące, gleba, Słońce, aparat rentgenowski, lekarstwa radioaktywne, dym papierosowy, telefon komórkowy, przewód z prądem, granit, gwiazdy, izotopowy miernik grubości, uliczna lampa sodowa, ciało człowieka, powietrze, ściany domów, woda
| Naturalne źródła promieniowania jonizującego | |
|---|---|
| Sztuczne źródła promieniowania jonizującego | |
| Elementy niepasujące do żadnej kategorii |
Do spowalniania neutronów w reaktorze jądrowym służy:
- moderator.
- chłodziwo, jeśli jest moderatorem.
- pręt kontrolny.
- reflektor.
- pręt paliwowy.
- betonowa osłona z dodatkiem boru.
- pręt bezpieczeństwa.
Który rodzaj promieniowania jonizującego jest najmniej przenikliwy?
- i
- i
- i promieniowanie rentgenowskie
- promieniowanie kosmiczne
- promieniowanie rentgenowskie
Poniższe równanie opisuje jedna z możliwych reakcji rozszczepienia jądra uranu:
.
Jaką wartość ma liczba neutronów wyzwolonych podczas tego procesu?
- 2
- 3
- 1
- 0
- 4
- Nie można policzyć liczby neutronów, ponieważ nie podano ilości energii wyzwolonej w tym procesie.
Chcąc wykryć promieniowanie jonizujące można posłużyć się:
- licznikiem Geigera-Müllera.
- komorą Wilsona.
- akceleratorem.
- cyklotronem.
- spektrografem.
- czytnikiem laserowym.
- wszystkimi wymienionymi przyrządami.
W elektrowni jądrowej energia pochodzi:
- z reakcji rozszczepienia jąder ciężkich izotopów.
- ze spalania izotopu uranu.
- ze spalania izotopu plutonu.
- z rozpadów α zachodzących w paliwie.
- z promieniowania jądrowego.
- z promieniowania kosmicznego.
Reakcje syntezy termojądrowej zachodzą:
- w centrach gwiazd, reaktorach termojądrowych oraz bombach wodorowych.
- wyłącznie w reaktorach jądrowych.
- w silnikach samochodowych na paliwo wodorowe.
- wyłącznie w gwiazdach.
- w bombie atomowej.
- wjądrze Ziemi.
Jakie funkcje pełnią poszczególne elementy reaktora jądrowego?
pochłaniają neutrony., spowalnia neutrony., chroni przed promieniowaniem., odprowadza ciepło z rdzenia reaktora., kieruje neutrony do rdzenia reaktora., ulega rozszczepieniu.
| Moderator | |
| Paliwo jądrowe | |
| Reflektor | |
| Pręty kontrolne | |
| Osłona biologiczna | |
| Chłodziwo |
Aby ochronić się przed szkodliwym działaniem promieniowania pochodzącego z zewnętrznego źródła wystarczy:
- zasłonić się grubą szybą ze szkła lub szkła organicznego.
- zasłonić się kartką papieru.
- zasłonić się grubą płytą ołowianą.
- zasłonić się grubą ścianą z betonu zawierającego dodatek boru.
Zadania
Oblicz energię wiązania jądra litu . Przyjmij, że jego masa wynosi ,
masa protonu jest równa , a masa neutronu to . Prędkość światła w próżni wynosi .
Okres połowicznego zaniku izotopu jodu stosowanego do badania tarczycy wynosi 8 dni. Oblicz, po ilu dniach aktywność preparatu podanego badanej osobie zmaleje 8 razy. Pomiń ubytek preparatu związany z jego wydalaniem go z organizmu.
Drewniany posążek znaleziony przez archeologów zawierał 4 razy mniej węgla niż próbka drewna pobrana z rosnącego obecnie drzewa. Oblicz wiek drewna, z którego wykonano posążek. Czas połowicznego zaniku węgla znajdź w dostępnych ci źródłach.
W opisie atomów i cząstek mniejszych od atomu masę wyraża się nie w kilogramach, ale w jednostkach masy atomowej (po angielsku unit), oznaczanych literą „” (). Oblicz deficyt masy jądra sodu . Masa tego jądra wynosi , masa protonu jest równa , a masa neutronu ma wartość . Obliczoną wartość deficytu masy podaj w kilogramach.
Tytoń, z którego produkuje się papierosy, zawiera dwa podstawowe izotopy promieniotwórcze: ołów i polon .
Podczas palenia papierosa polon, ulega sublimacji i prawie w całości przechodzi w dym papierosowy (popiół nie wykazuje aktywności promieniotwórczej). Aktywność promieniotwórcza dymu powstałego ze spalenia paczki papierosów wynosi około 200 mBq. Ile cząstek alfa emituje taki dym średnio w ciągu minuty?
Wymień, jakie narządy palacza narażone są na działanie tego promieniowania.
Gdyby aktywność dymu zmniejszyć czterokrotnie, to dawka promieniowania pochłaniana w ciągu roku przez osobę wypalającą dwie paczki papierosów dziennie osiągnęłaby wartość porównywalną z tą, jaką pochłonęli mieszkańcy wschodnich terenów Polski po katastrofie w Czarnobylu. Oblicz czas, po którym aktywność dymu zmalałaby cztery razy (zakładamy, że dym nie ulatnia się z pojemnika, w którym go przetrzymujemy do celów badawczych). Czas połowicznego zaniku dla izotopu wynosi = 138,4 dnia.