Grafika interaktywna
Polecenie 1
Zapoznaj się z poniższym doświadczeniem, przedstawionym krok po kroku za pomocą grafiki interaktywnej, a następnie rozwiąż ćwiczenia.
Jest to aromatyczny związek X, zawierający w cząsteczce m.in. 6 atomów węgla, który z wodnym roztworem chlorku żelaza(III) tworzy charakterystyczne zabarwienie. Jak wykazać doświadczalnie, że związek X wykazuje słabe właściwości kwasowe?
Grafika interaktywna pt. „Doświadczenie. Jak wykazać doświadczalnie, że związek X wykazuje słabe właściwości kwasowe?".
Źródło: GroMar Sp. z o.o. na podstawie M. Krzeczkowska, J. Loch, A. Mizera, Repetytorium chemia : Liceum - poziom podstawowy i rozszerzony, Wydawnictwo Szkolne PWN, Warszawa - Bielsko‑Biała 2010., licencja: CC BY-SA 3.0.
Ćwiczenie 1
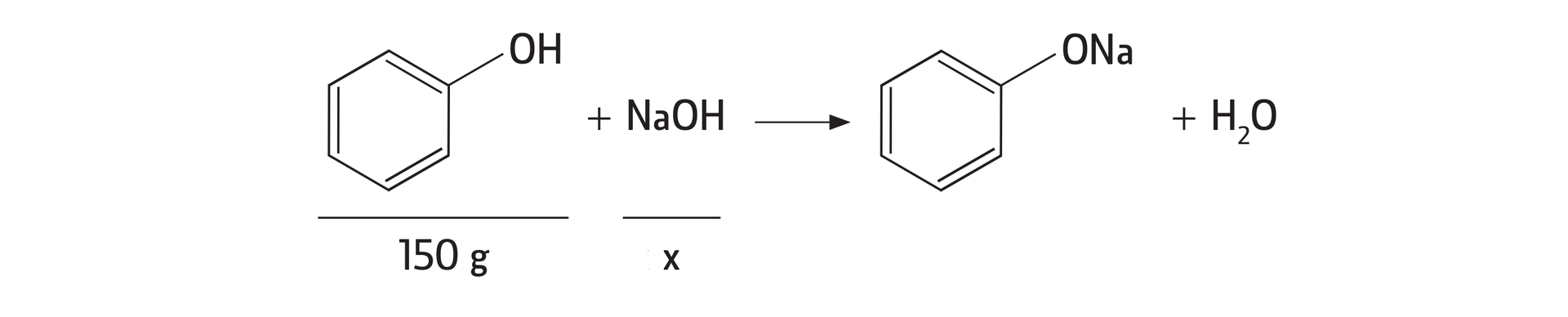
Ile g należy użyć do całkowitego zobojętnienia związku X z doświadczenia przedstawionego powyżej, zawartego w 150 g 2% roztworu?
Ćwiczenie 2
Opisz metodę wykrywania układu fenolowego.