Przeczytaj
Diagnostyka prenatalna to wszystkie badania wykonywane podczas ciąży, które mają określić, czy zarodek, a później płód, rozwija się prawidłowo. Pozwala ona na wczesne wykrycie wad, co stwarza szansę leczenia śródmacicznego w trakcie ciąży lub wykonania zabiegu u dziecka bezpośrednio po urodzeniu. Rozpoznanie wady pozwala również na odpowiednie przygotowanie do porodu matki oraz personelu medycznego.
Jakie choroby płodu można wykryć dzięki badaniom prenatalnym?
Rodzaje badań prenatalnych
Badania prenatalne w kierunku często występujących wad rozwojowych i nieprawidłowości genetycznych mogą mieć charakter nieinwazyjny lub inwazyjny. Metody nieinwazyjne nie ingerują bezpośrednio w środowisko płodu, a zatem nie wiążą się z ryzykiem powikłań w przebiegu ciąży. Stosuje się je u wszystkich kobiet ciężarnych, niezależnie od wieku. Jeśli na podstawie wyniku tych badań zostanie określone ryzyko wystąpienia wady, lekarz kieruje ciężarną na badania inwazyjne, wymagające dotarcia bezpośrednio do płodu.
Nieinwazyjne badania prenatalne
Badania nieinwazyjneBadania nieinwazyjne mają charakter przesiewowy, co oznacza, że badania te pozwalają oszacować ryzyko wystąpienia wad płodu. Oparte są na ocenie ultrasonograficznej płodu, a także na badaniu krwi ciężarnej. Są bezpieczne i dla dziecka, i dla matki. Charakterystykę poszczególnych nieinwazyjnych badań prenatalnych przedstawia poniższa tabela interaktywna.
Inwazyjne badania prenatalne
Badania inwazyjne mają charakter diagnostyczny, co oznacza, że pozwalają z dużym prawdopodobieństwem potwierdzić lub wykluczyć wadę płodu. Polegają na wykonaniu zabiegu, podczas którego pobierany jest materiał biologiczny pochodzący od płodu, przekazywany następnie do analiz laboratoryjnych i genetycznych. W zakresie badań inwazyjnych stosuje się:
amniopunkcję, czyli pobranie płynu owodniowego;
biopsję kosmówkikosmówki, czyli pobranie komórek łożyskałożyska;
kordocentezę, czyli pobranie krwi z żyły pępowinowej płodu.
Badania inwazyjne grożą powikłaniami zarówno u matki, jak i u płodu. W czasie zabiegu możliwe jest uszkodzenie łożyska lub pępowiny, nakłucie narządów płodu, a także zakażenie wewnątrzmaciczne.
Amniopunkcja
Amniopunkcja umożliwia wykrycie anomalii chromosomowych, dotyczących zarówno chromosomów płci (w zespole Turnera), jak i autosomów (w zespole Downa, Edwardsa), a także mutacji powodujących np. mukowiscydozę, anemię sierpowatą czy chorobę Huntingtona. Na podstawie testów biochemicznych wykonywanych na płynie owodniowym można wykryć groźne dla rozwoju płodu infekcje wirusowe i bakteryjne u matki, takie jak różyczka, kiła czy cytomegalia. Amniopunkcja jest również przydatna w wykrywaniu niegenetycznych zaburzeń rozwojowych, np. wad cewy nerwowej, powstających we wczesnych etapach rozwoju zarodka – przykładami takich schorzeń są wrodzony rozszczep kręgosłupa i przepuklina oponowo‑rdzeniowa.
Biopsja kosmówki
Analiza materiału genetycznego zawartego w komórkach kosmówki pozwala na wykrycie wad wynikających z anomalii chromosomowych. Biopsja kosmówkowa nie daje możliwości przeprowadzania testów na płynie owodniowym, jednak zaletą tej metody jest to, że można ją stosować już w 8–10 tygodniu ciąży, a wyniki otrzymuje się w ciągu jednego dnia.
Kordocenteza
Wskazania do inwazyjnych badań prenatalnych
Fetoskopia jest metodą umożliwiającą przeprowadzanie interwencji medycznych u płodu, takich jak biopsja, laserowe zamknięcie nieprawidłowych naczyń krwionośnych czy chirurgiczne leczenie rozszczepu kręgosłupa. Polega na wprowadzeniu przez powłoki brzuszne i ścianę macicy do jamy owodniowej fetoskopu – jest to cienka rurka zawierająca kamerę i światłowody, pozwalające na obserwację i wykonywanie zdjęć wnętrza macicy oraz pobieranie próbek tkanek i płynów. Za jej pośrednictwem wprowadza się również narzędzia chirurgiczne, np. włókna laserowe służące do wykonywania zabiegów. Badanie fetoskopowe jest wysoce ryzykowne dla płodu, dlatego przeprowadza się je głównie w celach terapeutycznych, a nie diagnostycznych. Dzięki tej metodzie możliwe jest wykonywanie w łonie matki np. zabiegów ograniczających wady rozszczepu kręgosłupa z przepukliną oponowo‑rdzeniową, operacji usunięcia guzów nowotworowych oraz przetaczania krwi w przypadku ryzyka wystąpienia choroby hemolitycznejchoroby hemolitycznej. Zabiegi te można przeprowadzać między 18 a 20 tygodniem ciąży.
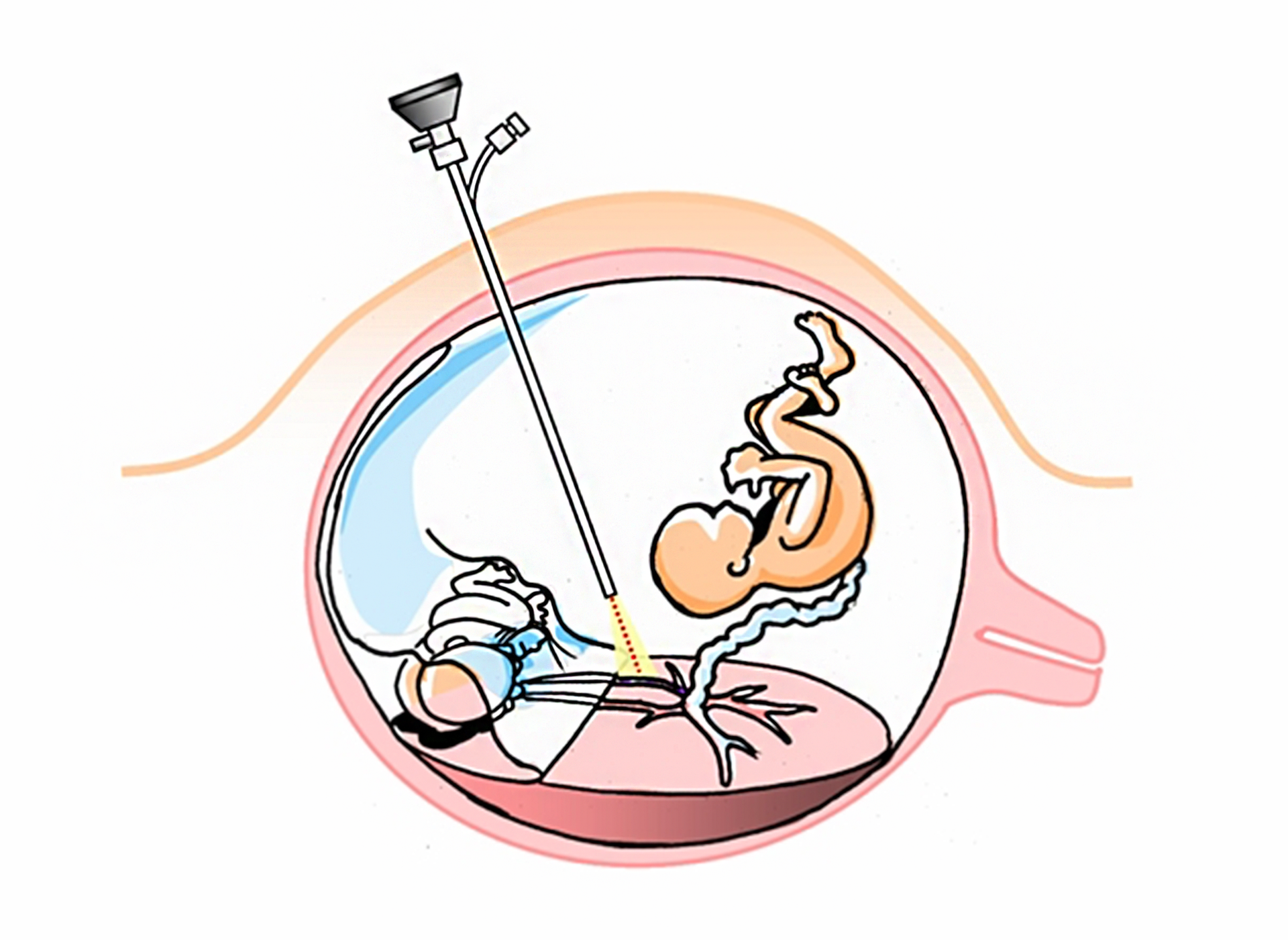
Fetoskopia wykorzystywana jest również w przypadku powikłania ciąży mnogiej, zwanego zespołem przetoczenia krwi między płodami. Powikłanie to grozi bliźniętom, które mają wspólne łożysko, i polega na nieprawidłowym przepływie krwi między płodami, w wyniku czego jeden z nich otrzymuje zbyt małe ilości tlenu i składników pokarmowych, a drugi – ich nadmierne ilości. Wówczas za pomocą fetoskopu wprowadza się włókno laserowe do jamy macicy i niszczy te naczynia, które w łożysku łączą krwiobiegi bliźniąt. Taka operacja stwarza szansę na przeżycie obu płodów.
Słownik
zmiany kariotypukariotypu człowieka w zakresie liczby chromosomów lub ich struktury
badania, które pozwalają określić ryzyko wystąpienia wady płodu; zaleca się je każdej kobiecie ciężarnej
choroba, która jest wynikiem tzw. konfliktu serologicznego, czyli reakcji między przeciwciałami IgG matki a antygenami krwinek płodu; występuje, gdy matka ma grupę krwi RhIndeks górny −−, a dziecko RhIndeks górny ++
(gr. karyon – orzeszek, jądro; týpos – odbicie, obraz) kompletny zestaw chromosomów komórki somatycznej organizmu; jest cechą charakterystyczną dla osobników tego samego gatunku tej samej płci; wyróżnia się w nim chromosomy nieróżniące się u osobników różnych płci – autosomy oraz chromosomy płci – allosomy; prawidłowy kariotyp człowieka składa się z 22 par autosomów oraz 1 pary chromosomów płci oznaczanych symbolami X i Y (XX u kobiet i XY u mężczyzn)
(łac. chorion) – najbardziej zewnętrzna błona płodowa, pośrednicząca między zarodkiem a środowiskiem zewnętrznym; u ssaków jest częścią łożyska, które dostarcza tlen i substancje odżywcze, a usuwa zbędne produkty przemiany materii
(łac. placenta) – tymczasowy narząd w macicy ssaków, który tworzy połączenie między układami krążenia matki i dziecka; umożliwia zaopatrzenie płodu w tlen oraz substancje pokarmowe i jednocześnie usuwa szkodliwe produkty przemiany materii; wytwarza hormony podtrzymujące ciążę; oprócz składników pokarmowych do krwi płodu mogą przedostawać się przeciwciała, niektóre wirusy, antybiotyki i szkodliwe substancje, np. alkohol, narkotyki
utrata jednego chromosomu z pary homologicznej; jest wynikiem mutacji wywołanej nieprawidłową segregacją chromosomów w czasie podziału komórki; wszystkie takie mutacje autosomów są śmiertelne; monosomia chromosomów płci typu X0 objawia się jako zespół Turnera
obecność dodatkowego, trzeciego chromosomu w określonej parze homologicznej; jest wynikiem mutacji wywołanej nieprawidłową segregacją chromosomów w czasie podziału komórki
(z łac. prae – przed i natalis – urodzeniowy) – w rozwoju osobniczym ssaków łożyskowych okres od zapłodnienia komórki jajowej do narodzin dziecka
(gr. trophé – pokarm, blastós – kiełek, zarodek) – warstwa zewnętrznych komórek kosmówki (błona płodowa), odpowiedzialna za powstawanie łożyska
(łac. in vitro – dosł. w szkle) – sztuczne zapłodnienie, zapłodnienie pozaustrojowe; metoda połączenia żeńskiej komórki rozrodczej z komórką rozrodczą męską w warunkach laboratoryjnych; w jego wyniku powstaje zygota rozwijająca się w zarodek; metoda leczenia niepłodności zaliczana do technik rozrodu wspomaganego medycznie