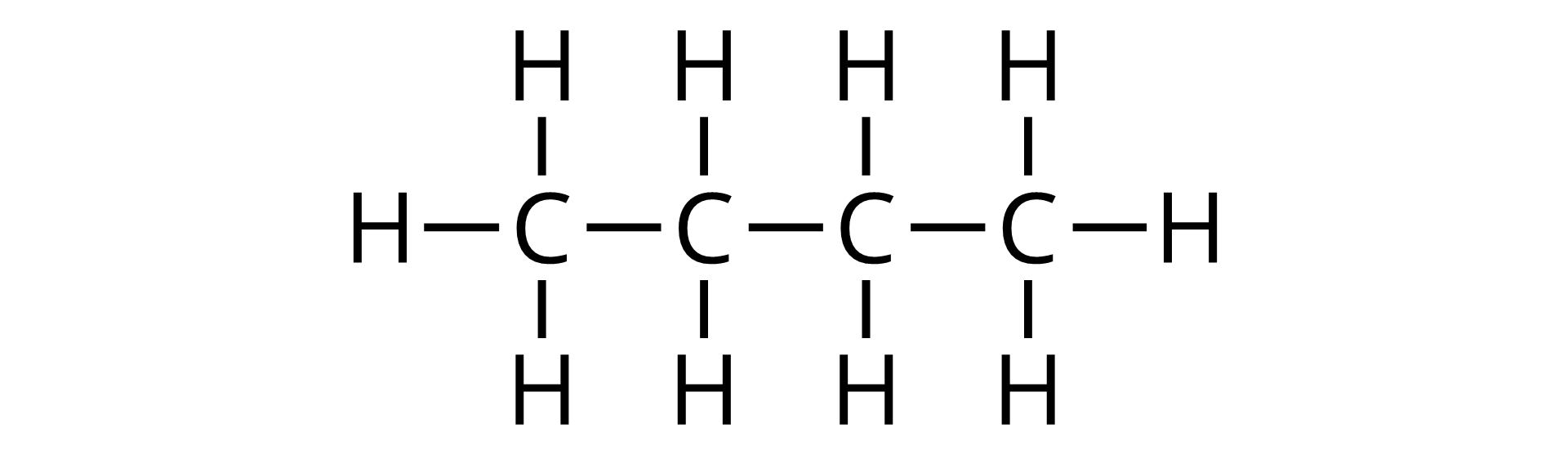Przeczytaj
Aby dobrze zrozumieć tematy dotyczące węglowodorów, należy znać podstawowy zestaw informacji ogólnych na ich temat. Po przypomnieniu sobie potrzebnych informacji przejdź do pracy z materiałem.
Ogólny podział węglowodorów
Węglowodory dzielą się na wiele różnych kategorii, co potwierdza przedstawiony powyżej schemat. W tej lekcji zdobędziesz wiedzę szczegółową na temat jednej z rodzin węglowodorów, czyli alkanówalkanów, które należą do węglowodorów łańcuchowych nasyconych.
Jak zbudowane są cząsteczki alkanów?
Alkany są przedstawicielami węglowodorów alifatycznych. Są to nasycone związki organiczne, których cząsteczki zbudowane są wyłącznie z atomów węgla i wodoru o wzorze ogólnym:
Gdzie „” oznacza liczbę atomów węgla w cząsteczce.
Alkany posiadają budowę łańcuchową. Tworzą one łańcuchy proste oraz rozgałęzione.
Alkany o łańcuchach prostych
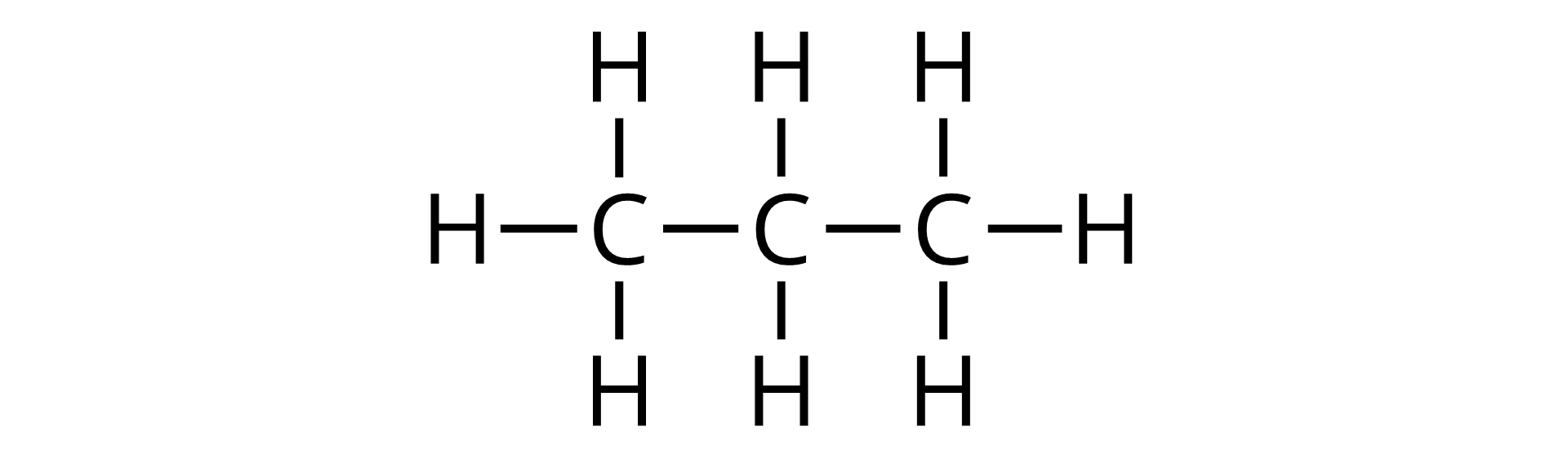
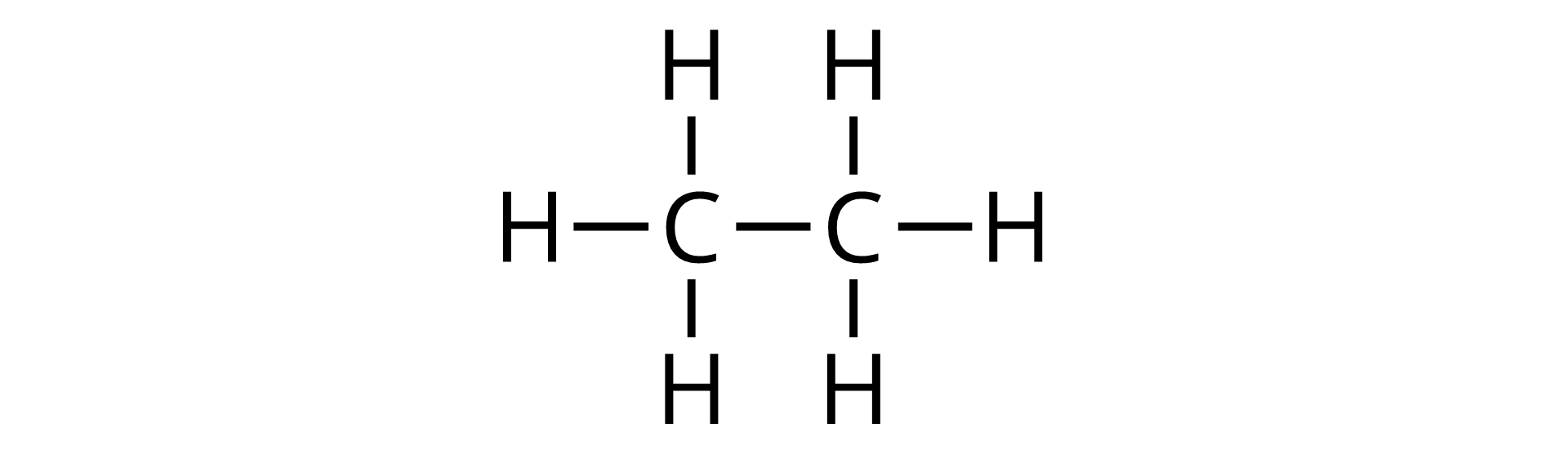
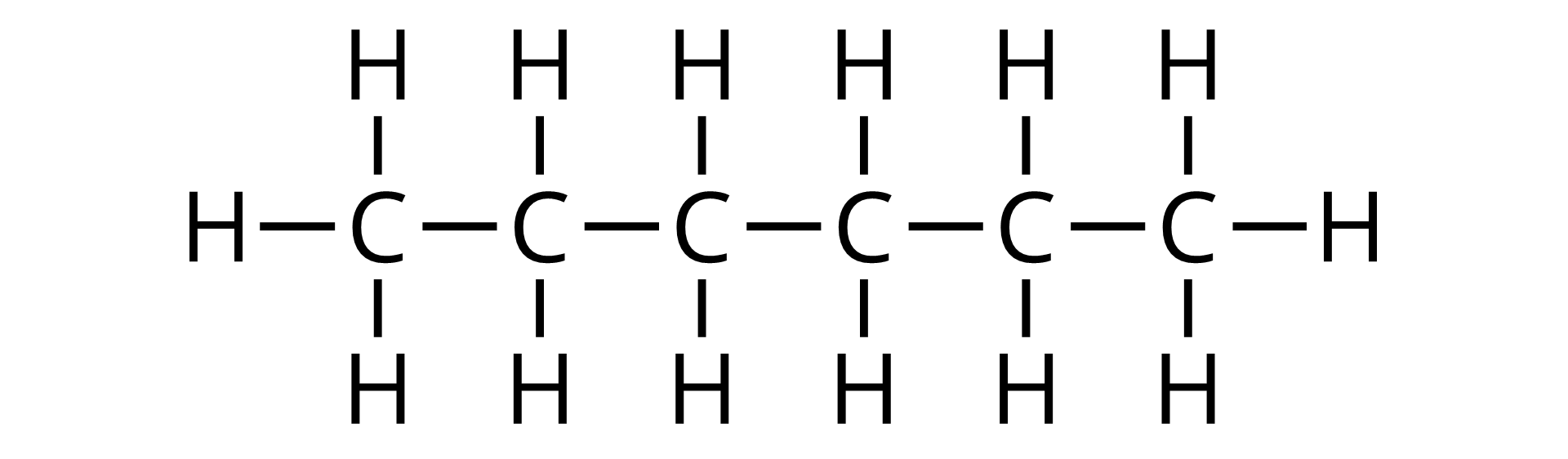
Łańcuchy w węglowodorach mogą być krótkie lub dłuższe, co związane jest z liczbą atomów węgla obecnych w cząsteczce danego alkanu.
Na podstawie powyższych modeli znajdź stały, powtarzalny, identyczny fragment, który jest wspólny dla budowy każdego z tych alkanów.
Alkany tworzą szereg homologiczny o wzorze ogólnym: . Poszczególne człony szeregu, zwane homologami, różnią się o taki sam element strukturalny () lub jego krotność.
Liczba atomów węgla | Nazwa alkanu | Wzór sumaryczny | Wzór półstrukturalny |
|---|---|---|---|
1 | metan | ||
2 | etan | ||
3 | propan | ||
4 | butan | ||
5 | pentan | ||
6 | heksan | ||
7 | heptan | ||
8 | oktan | ||
9 | nonan | ||
10 | dekan |
W nawiązaniu do powyższej tabeli, zapisz wzór sumaryczny kolejnego węglowodoru z szeregu homologicznego.
Pamiętaj, że znając wzór ogólny szeregu homologicznego alkanów oraz liczbę atomów węgla w cząsteczce możemy obliczyć liczbę atomów wodoru i odwrotnie - potrafimy także obliczyć liczbę atomów węgla, znając liczbę atomów wodoru.
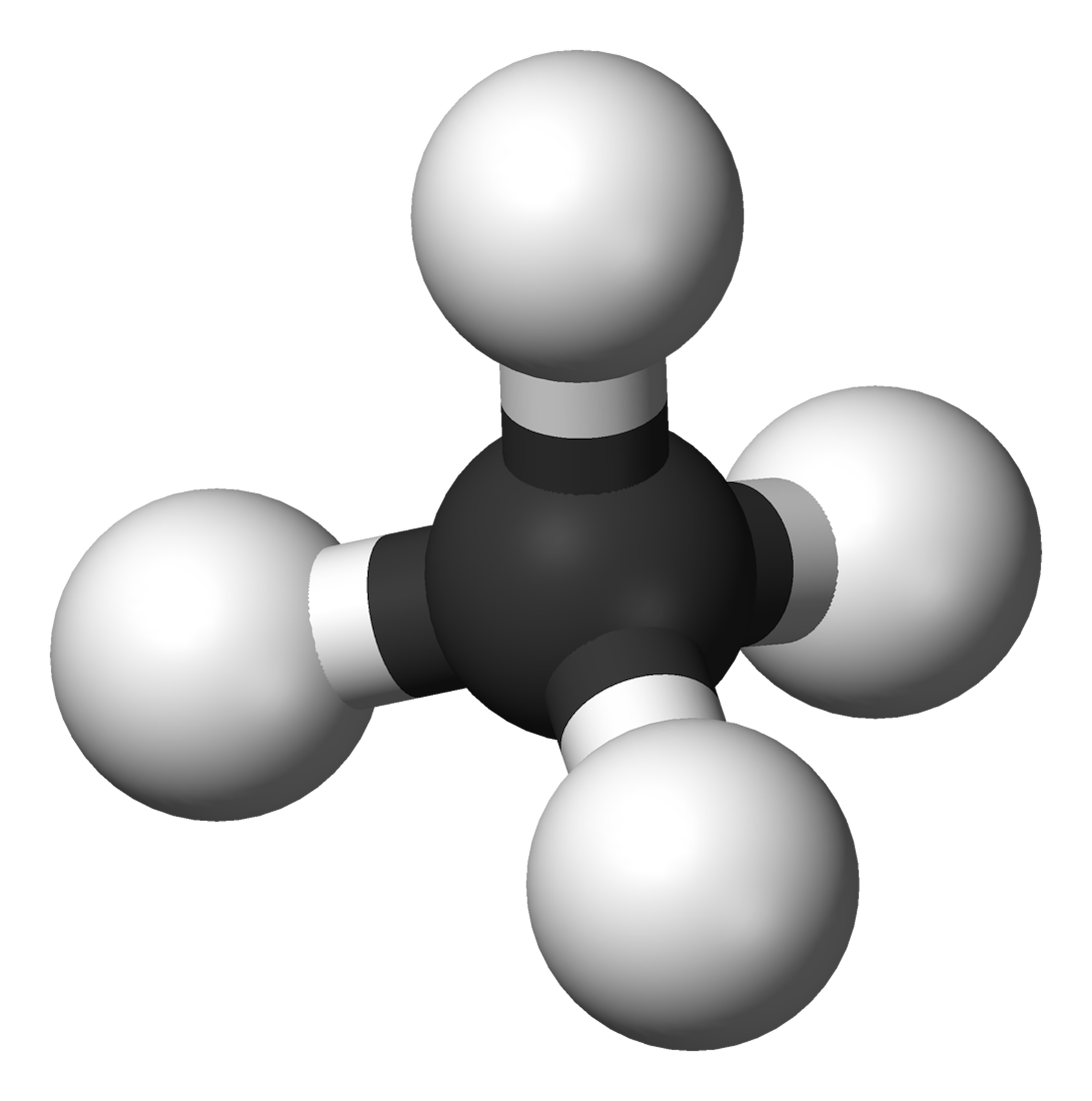
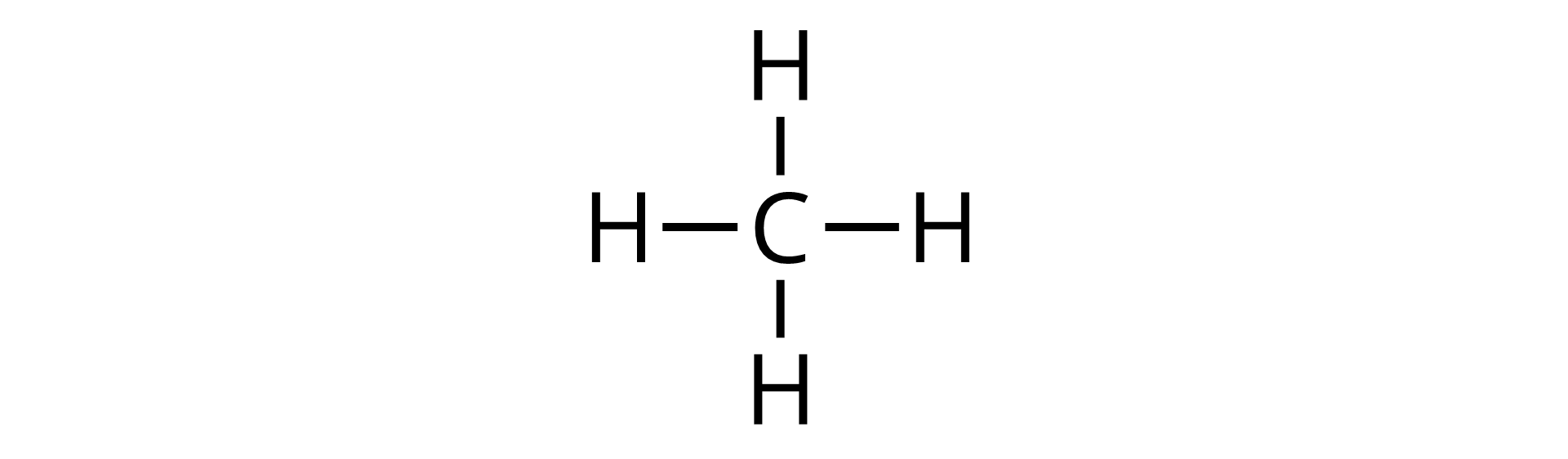
Pierwszym przedstawicielem szeregu homologicznego alkanów jest węglowodór o nazwie metan.
Cząsteczka metanu zbudowana jest tylko z jednego atomu węgla. Atom węgla posiada 4 elektrony walencyjne, w związku może utworzyć maksymalnie cztery wiązania chemiczne. W cząsteczce metanu poza 1 atomem węgla są obecne jeszcze 4 atomy wodoru.
Wzór strukturalny jest podstawowym sposobem przedstawienia struktury danego węglowodoru; ukazuje rodzaj i liczbę atomów w cząsteczce oraz ich kolejność i sposób powiązania. W chemii stosuje się także wzory przestrzenne, które dodatkowo prezentują wzajemną orientację przestrzenną atomów w cząsteczce, dlatego są przydatne w ukazywaniu trójwymiarowej złożoności węglowodorów. Wzory strukturalne złożonych związków organicznych często zapisywane są przy użyciu wzorów szkieletowych, w których pomija się symbole literowe atomów węgla i wodoru, występujące w głównym szkielecie cząsteczki.
Wzory strukturalne wybranych alkanów
Alkany o łańcuchach rozgałęzionych
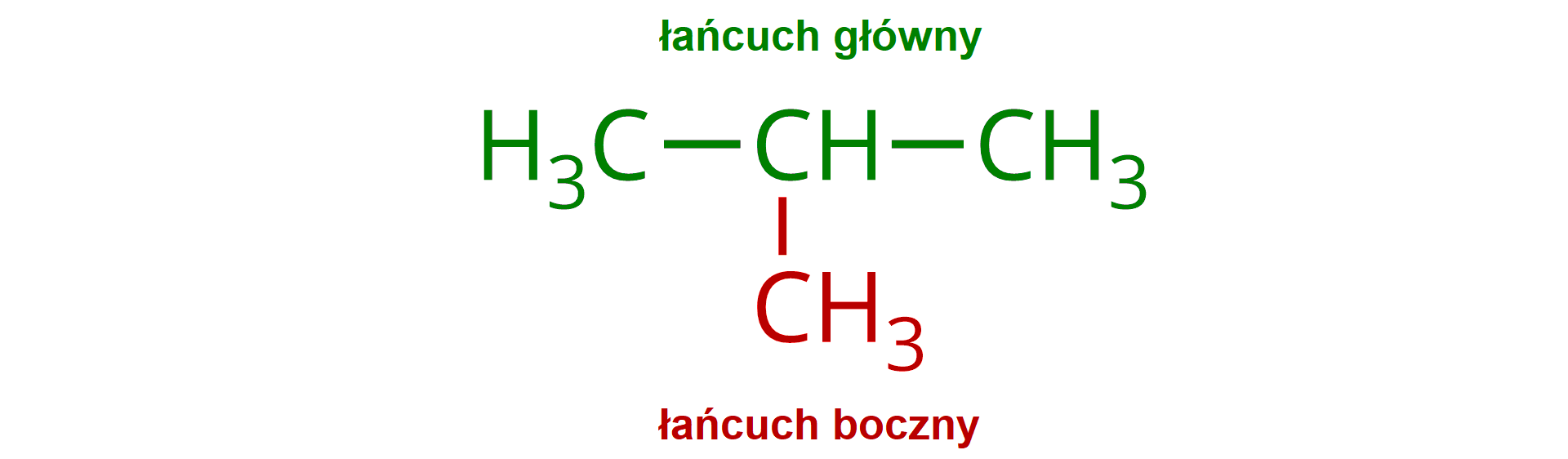
O alkanach z łańcuchami rozgałęzionymi mówimy wtedy, gdy do alkanu o łańcuchu prostym dołączony został podstawnik (rodnik alkilowy) lub podstawniki - czyli są tzw. łańcuchy boczne w cząsteczce. Alkil jest jednowartościowy i powstaje przez oderwanie jednego atomu wodoru od cząsteczki alkanu (wzór ogólny ), np. grupa metylowa (metyl) , grupa etylowa (etyl) .
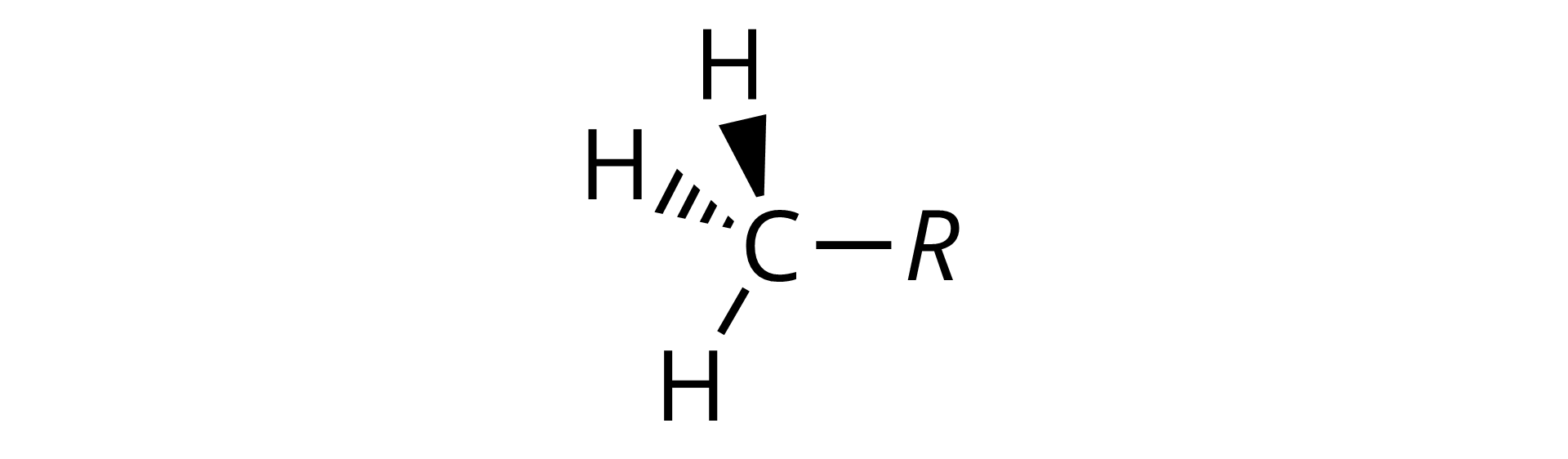
W chemii organicznej wzór sumaryczny ma mniejsze zastosowanie, z uwagi na to, że niewiele mówi o strukturze cząsteczek. Natomiast wzór strukturalny w przypadku dużych cząsteczek staje się niewygodny w użyciu. Używa się więc wzoru półstrukturalnego. Dla cząsteczek węglowodorów, pisząc wzór półstrukturalny, przedstawia się tylko połączenia pomiędzy atomami węgla, natomiast nie rozpisuje się wiązań pomiędzy atomami węgla i wodoru.
Wiązania
Ze względu na typ i krotność wiązań między atomami węgla w cząsteczce, alkany należą do węglowodorów łańcuchowych nasyconych.
Krotność wiązań
Alkany to grupa węglowodorów nasyconych. Swój nasycony charakter zawdzięczają obecności wyłącznie wiązań pojedynczych pomiędzy atomami.
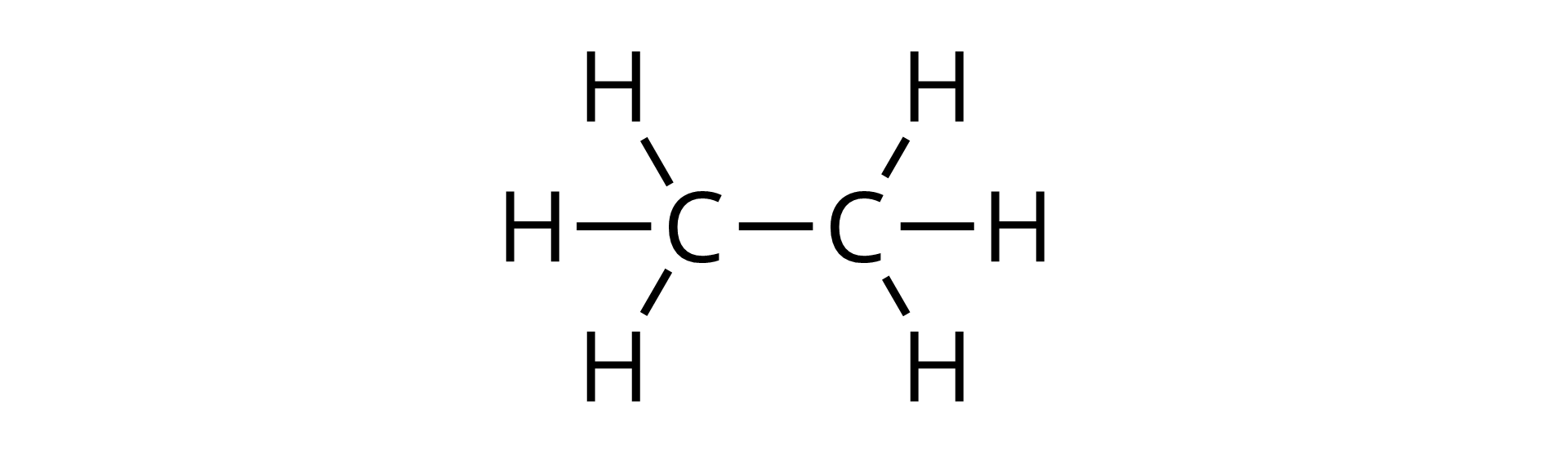
Źródło: GroMar Sp. z o.o., licencja: CC BY-SA 3.0.
Typ wiązania
W węglowodorach mogą występować wiązania typu sigma (σ) i pi (π). W cząsteczkach alkanów występują tylko wiązania pojedyncze zarówno między atomami węgla, jak i atomami węgla i atomami wodoru; są to wiązania typu sigma.
Hybrydyzacja
Orbitale walencyjne atomów węgla w cząsteczkach alkanów występują w stanie hybrydyzacjihybrydyzacji spIndeks górny 33.
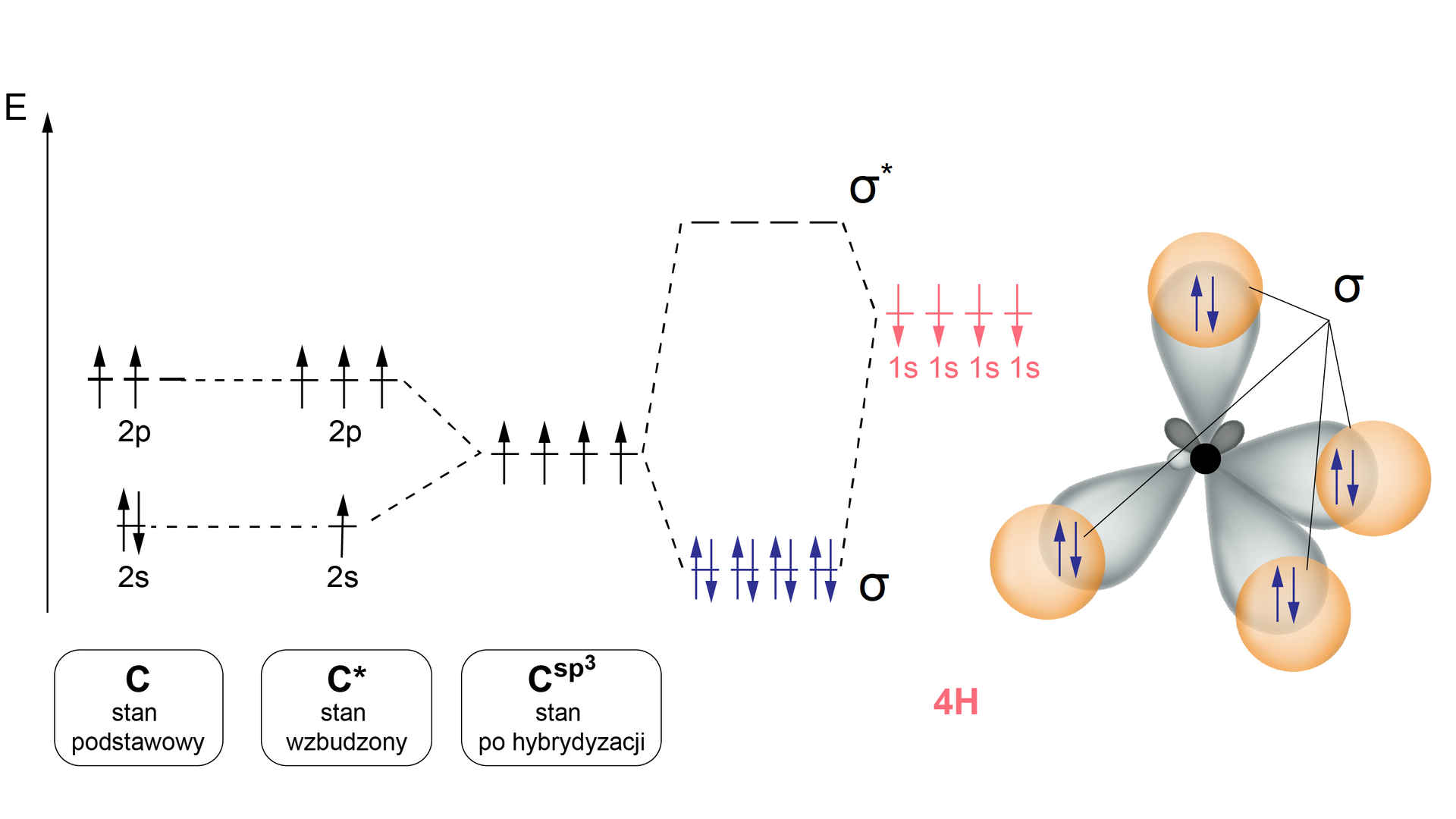
Każda hybryda jest wynikiem mieszania się 1 orbitalu typu s oraz 3 orbitali p. Orbitale zhybrydyzowane (hybrydy) ułożone są w przestrzeni do naroży czworościanu foremnegoczworościanu foremnego (tetraedr), a kąty pomiędzy wiązaniami wynoszą 109,5°.
Atomy węgla połączone są ze sobą wyłącznie wiązaniami pojedynczymi typu sigma. Długość wiązania pojedynczego węgiel‑węgiel wynosi 154 pm, a energia wiązania 368 .
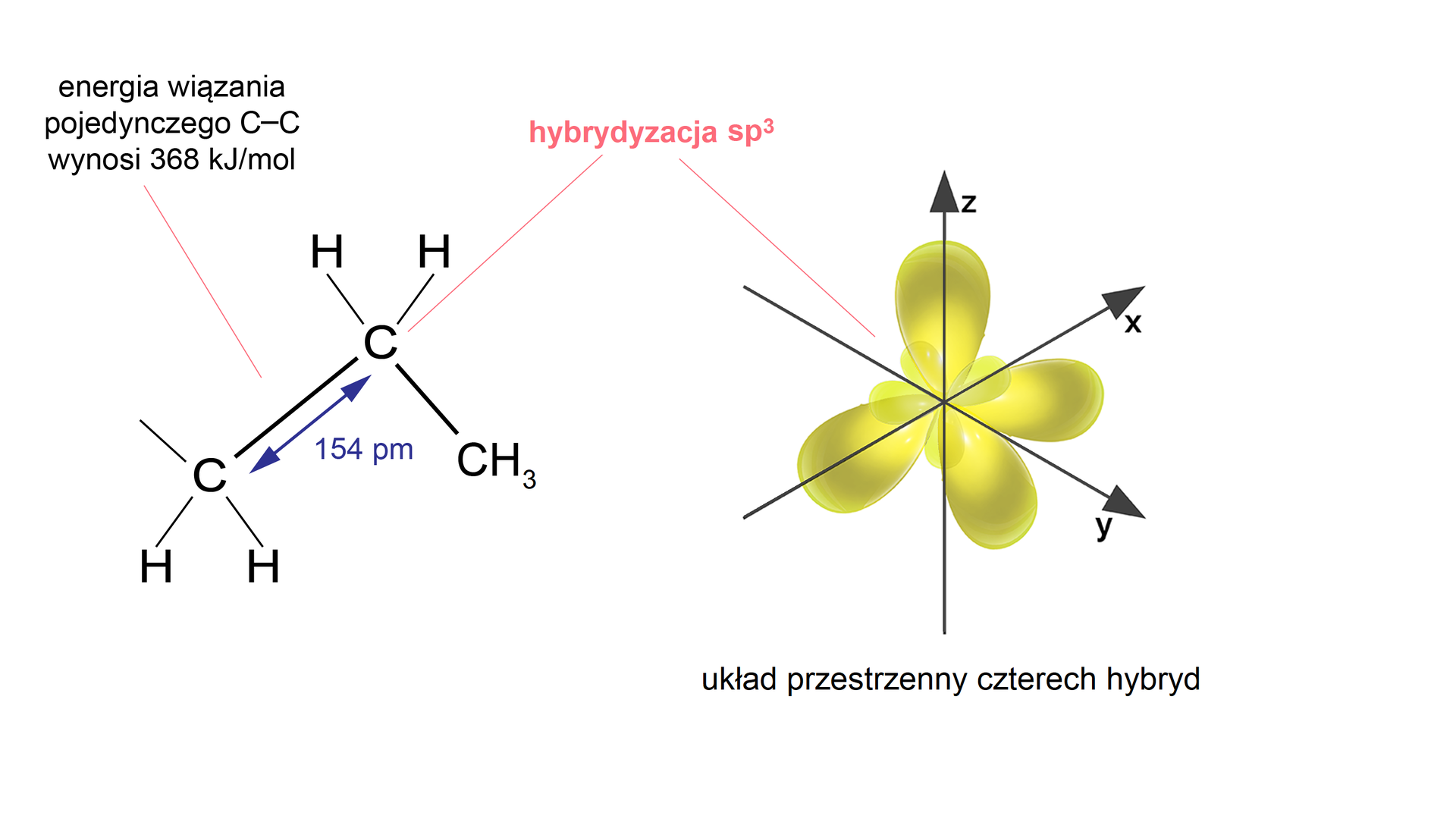
Poniżej przedstawiono schemat nakładania orbitali atomowych oraz model kulkowy cząsteczki etanu.
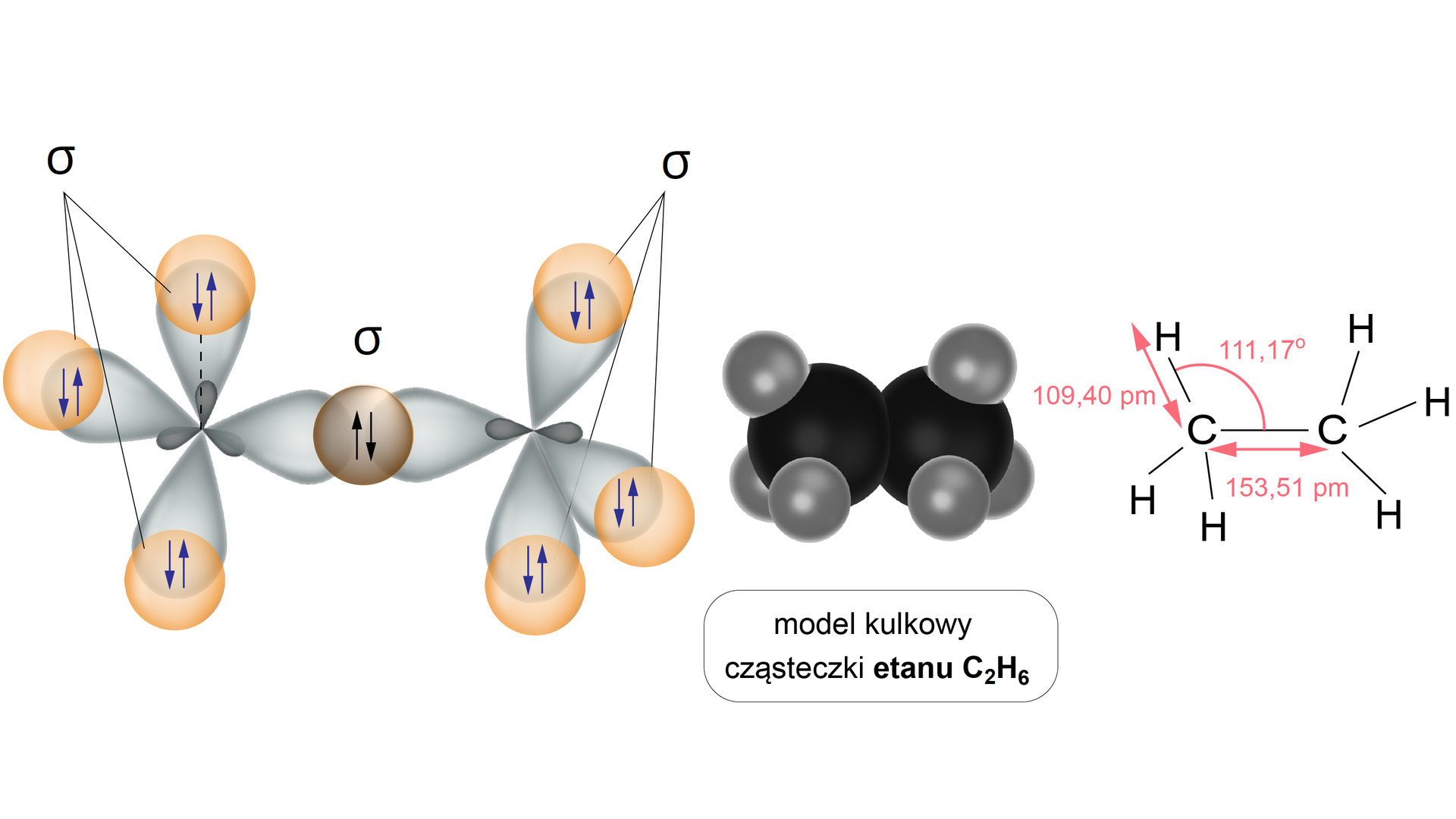
Izomeria
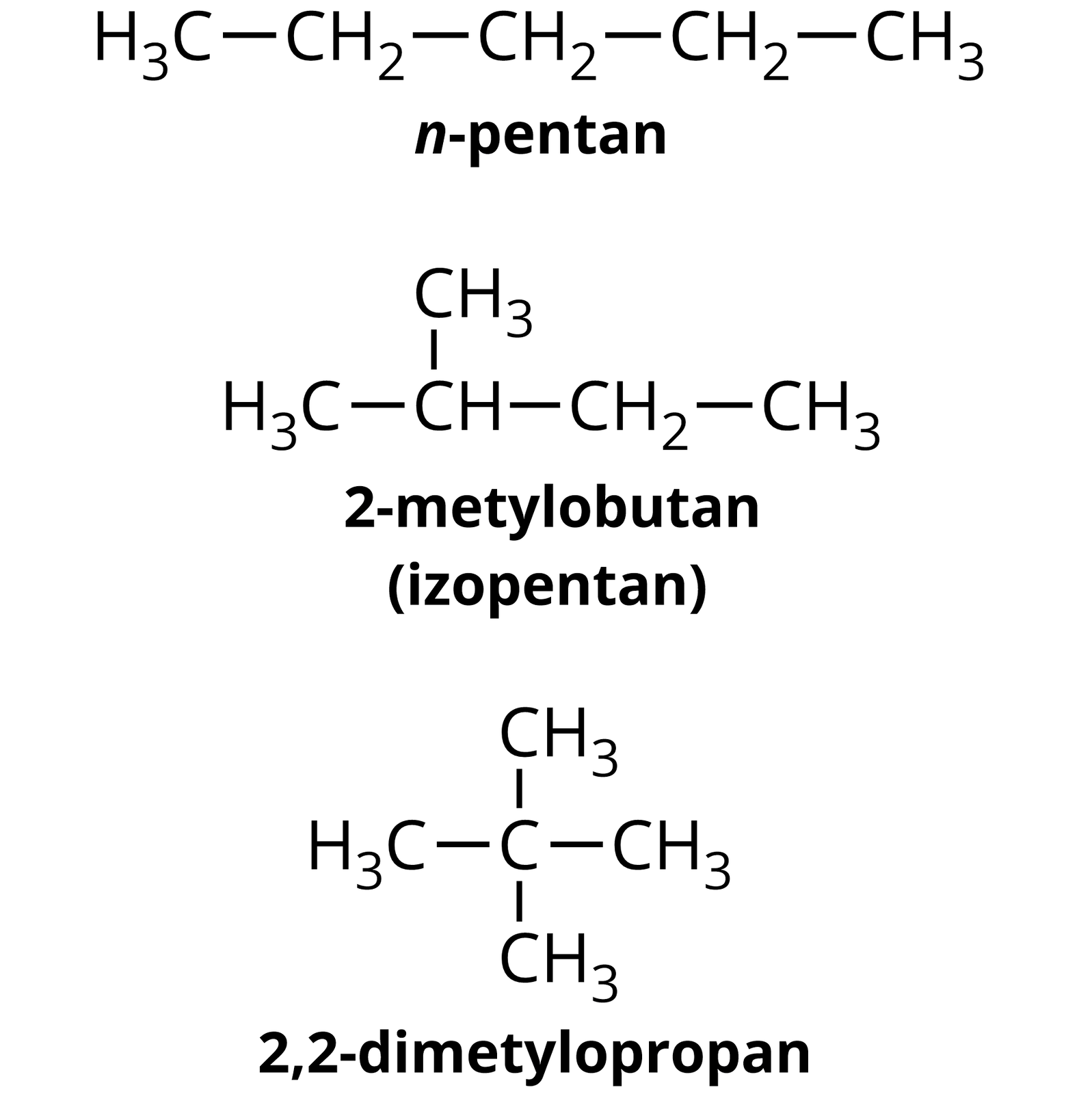
Alkany to związki chemiczne tworzące – począwszy od butanu – izomery. Możliwość tworzenia izomerów związana jest z tym, że alkany mogą występować w formie rozgałęzionej, która ma taki sam wzór sumaryczny, jak jej prostoliniowy odpowiednik, jednak atomy w cząsteczce połączone są ze sobą w innej kolejności. Ten typ izomerii określa się mianem izomerii konstytucyjnej. Z racji, że alkany występują wyłącznie w postaci łańcuchowej i nie tworzą związków cyklicznych, izomeria konstytucyjna występująca w tych węglowodorach nosi nazwę izomerii szkieletowej łańcuchowej.
Jaką budowę łańcucha węglowego może mieć alkan posiadający 5 atomów węgla? Ile różnych izomerów może utworzyć? Czy potrafisz zapisać ich wzory półstrukturalne?
Niektóre alkany wykazują również izomerię przestrzenną, czyli stereoizomerię. Stereoizomery to związki o identycznym wzorze strukturalnym (zatem atomy są ze sobą połączone w tej samej kolejności), jednak mają one inne ułożenie w przestrzeni. Rozważmy 3‑metyloheksan, który tworzy dwa stereoizomery, gdyż trzeci atom węgla może występować w konfiguracji S lub w konfiguracji R.

Innym przykładem stereoizomerii występującej w alkanach jest tzw. izomeria konformacyjna. Jej występowanie wynika z faktu, że atomy węgla w alkanach są ze sobą połączone wiązaniami pojedynczymi i istnieje możliwość obrotu atomów lub grup atomów połączonych z sąsiednimi atomami węgla wokół wiązania sigma. Powoduje to, że ta sama cząsteczka może mieć atomy różnie zorientowane względem siebie w przestrzeni (dotyczy to stanu gazowego i ciekłego węglowodoru). Oznacza to, że istnieją różne konformacjekonformacje przestrzenne tej samej cząsteczki.
Niektóre powstałe w ten sposób struktury są jednak nietrwałe. Stosunkowo trwałą konformację nazywamy konformerem.

Słownik
(łac. parum affinis „mało powinowany”) nasycone węglowodory, czyli związki organiczne zbudowane z atomów węgla i atomów wodoru, o wzorze ogólnym posiadają w swojej strukturze wyłącznie wiązania pojedyncze między atomami
zabieg matematyczny polegający na utworzeniu równocennych energetycznie orbitali atomowych (tzw. hybryd) wskutek „zmieszania”/”uśredniania” orbitali atomowych odpowiednich typów
szereg związków organicznych należących do jednej grupy, których struktura zmienia się w stosunku do poprzedniego o pojedynczy, identyczny fragment – grupę metylenową
wielościan o czterech przystających ścianach, które są trójkątami równobocznymi



układ przestrzenny atomów w cząsteczce węglowodoru, który zmienia się w wyniku swobodnego obrotu wokół pojedynczych wiązań chemicznych, bez ich pękania; w cząsteczkach dłuższych alkanów następuje stale trwająca rotacja grup, ale jest ograniczona w momencie, gdy spowodowałaby nakładanie się poszczególnych atomów w przestrzeni
Bibliografia
Atkins P., Jones L. Chemia ogólna. Cząsteczki, materia, reakcje, Warszawa 2004, s. 524‑525.
Mastalerz P., Podręcznik chemii organicznej, Wrocław 1998.
McMurry J., Chemia organiczna, t. 2, Warszawa 2000.
Morrison R. T., Boyd R. N., Chemia organiczna, t. 1‑2, Warszawa 1997.